Die nichtalkoholische Fettlebererkrankung (NAFLD) ist heute die Hauptursache für chronische Lebererkrankungen in China und weltweit. Das Krankheitsspektrum umfasst die einfache Steatohepatitis, die nichtalkoholische Steatohepatitis (NASH) sowie die damit verbundenen Formen der Leberzirrhose und Leberkrebs. NASH ist durch übermäßige Fettansammlung in den Leberzellen und dadurch verursachte Zellschäden und Entzündungen gekennzeichnet, mit oder ohne Leberfibrose. Der Schweregrad der Leberfibrose bei NASH-Patienten ist eng mit einer schlechten Leberprognose (Zirrhose und ihre Komplikationen sowie hepatozelluläres Karzinom), Herz-Kreislauf-Erkrankungen, extrahepatischen Malignomen und Tod jeglicher Ursache verbunden. NASH kann die Lebensqualität der Patienten beeinträchtigen; es gibt jedoch noch keine zugelassenen Medikamente oder Therapien zur Behandlung von NASH.
Eine kürzlich im New England Journal of Medicine (NEJM) veröffentlichte Studie (ENLIVEN) zeigte, dass Pegozafermin sowohl die Leberfibrose als auch die Leberentzündung bei durch Biopsie bestätigten nicht-zirrhotischen NASH-Patienten verbesserte.
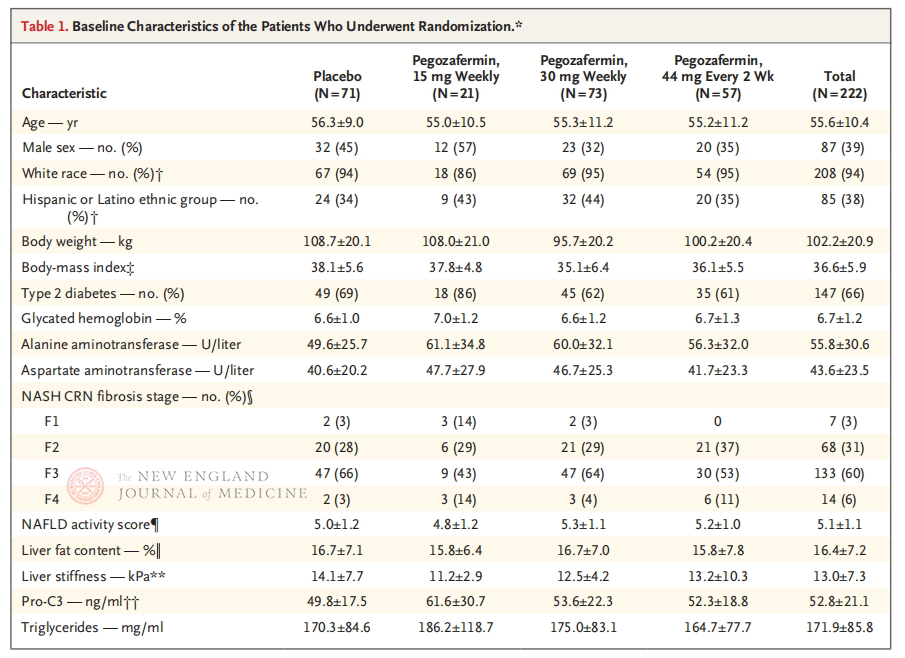
An der multizentrischen, randomisierten, doppelblinden, placebokontrollierten klinischen Phase-2b-Studie, die von Professor Rohit Loomba und seinem klinischen Team an der University of California, San Diego School of Medicine, durchgeführt wurde, nahmen zwischen dem 28. September 2021 und dem 15. August 2022 222 Patienten mit biopsiebestätigter NASH im Stadium F2-3 teil. Sie wurden randomisiert entweder Pegozafermin (subkutane Injektion, 15 mg oder 30 mg einmal wöchentlich oder 44 mg einmal alle 2 Wochen) oder Placebo (einmal wöchentlich oder einmal alle 2 Wochen) zugeteilt. Primäre Endpunkte waren eine Verbesserung der Fibrose ab Stadium 1 und keine Progression der NASH. Die NASH heilte ohne fibrotische Progression ab. Im Rahmen der Studie wurde auch eine Sicherheitsbewertung durchgeführt.
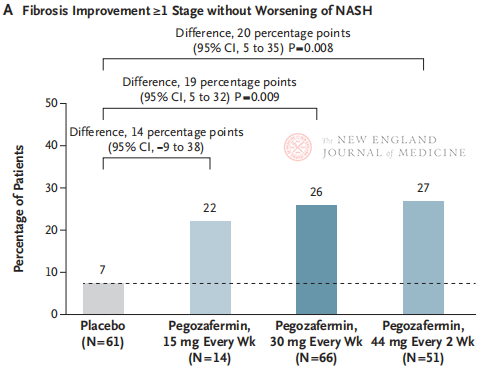
Nach 24-wöchiger Behandlung war der Anteil der Patienten mit einer Verbesserung der Fibrose im Stadium 1 oder höher und ohne Verschlechterung der NASH sowie der Anteil der Patienten mit einer Regression der NASH und ohne Verschlechterung der Fibrose in den drei Pegozafermin-Dosisgruppen signifikant höher als in der Placebogruppe. Signifikantere Unterschiede gab es bei Patienten, die einmal alle zwei Wochen 44 mg oder einmal wöchentlich 30 mg erhielten. In Bezug auf die Sicherheit war Pegozafermin einem Placebo ähnlich. Die häufigsten Nebenwirkungen der Pegozafermin-Behandlung waren Übelkeit, Durchfall und Erythem an der Injektionsstelle. Vorläufige Ergebnisse dieser Phase-2b-Studie deuten darauf hin, dass die Behandlung mit Pegozafermin die Leberfibrose verbessert.
Das in dieser Studie verwendete Pegozafermin ist ein lang wirkendes Glykosilanalogon des humanen Fibroblasten-Wachstumsfaktors 21 (FGF21). FGF21 ist ein endogenes Stoffwechselhormon, das von der Leber ausgeschüttet wird und eine Rolle bei der Regulierung des Lipid- und Glukosestoffwechsels spielt. Frühere Studien haben gezeigt, dass FGF21 therapeutische Wirkungen auf NASH-Patienten hat, indem es die Insulinsensitivität der Leber erhöht, die Fettsäureoxidation stimuliert und die Lipogenese hemmt. Die kurze Halbwertszeit von natürlichem FGF21 (ca. 2 Stunden) schränkt jedoch seinen Einsatz in der klinischen Behandlung von NASH ein. Pegozafermin nutzt die glykosylierte Pegylierungstechnologie, um die Halbwertszeit von natürlichem FGF21 zu verlängern und seine biologische Aktivität zu optimieren.
Zusätzlich zu den positiven Ergebnissen dieser klinischen Studie der Phase 2b zeigte eine weitere kürzlich in Nature Medicine veröffentlichte Studie (ENTRIGUE), dass Pegozafermin auch Triglyceride, Nicht-HDL-Cholesterin, Apolipoprotein B und Leberverfettung bei Patienten mit schwerer Hypertriglyceridämie signifikant senkte, was sich positiv auf die Verringerung des Risikos kardiovaskulärer Ereignisse bei Patienten mit NASH auswirken könnte.
Diese Studien deuten darauf hin, dass Pegozafermin als endogenes Stoffwechselhormon Patienten mit NASH vielfältige metabolische Vorteile bieten kann, insbesondere da NASH künftig möglicherweise in metabolisch assoziierte Fettlebererkrankung umbenannt wird. Diese Ergebnisse machen es zu einem sehr wichtigen potenziellen Medikament zur Behandlung von NASH. Gleichzeitig werden diese positiven Studienergebnisse Pegozafermin in klinischen Studien der Phase 3 unterstützen.
Obwohl sowohl die zweiwöchentliche Behandlung mit 44 mg Pegozafermin als auch die wöchentliche Behandlung mit 30 mg Pegozafermin den histologischen primären Endpunkt der Studie erreichte, betrug die Behandlungsdauer in dieser Studie nur 24 Wochen, und die Compliance-Rate in der Placebogruppe lag bei nur 7 %, was deutlich unter den Ergebnissen früherer klinischer Studien mit einer Dauer von 48 Wochen lag. Sind die Unterschiede und die Sicherheit gleich? Angesichts der Heterogenität der NASH sind in Zukunft größere, multizentrische, internationale klinische Studien erforderlich, um größere Patientenpopulationen einzubeziehen und die Behandlungsdauer zu verlängern, um die Wirksamkeit und Sicherheit des Medikaments besser bewerten zu können.
Veröffentlichungszeit: 16. September 2023