Die gemischte Hyperlipidämie ist durch erhöhte Plasmaspiegel von Low-Density-Lipoproteinen (LDL) und triglyceridreichen Lipoproteinen gekennzeichnet, was bei dieser Patientengruppe zu einem erhöhten Risiko für atherosklerotische Herz-Kreislauf-Erkrankungen führt.
ANGPTL3 hemmt Lipoproteinlipase und Endosepiase sowie die Aufnahme triglyceridreicher Lipoproteine in die Leber. Träger der inaktivierten ANGPTL3-Variante wiesen niedrigere Triglycerid-, LDL-Cholesterin-, HDL-Cholesterin- und Nicht-HDL-Cholesterinwerte auf und hatten ein geringeres Risiko für atherosklerotische Herz-Kreislauf-Erkrankungen. Zodasiran ist ein Small Interfering RNA (RNAi)-Medikament, das auf die ANGPTL3-Expression in der Leber abzielt.
Bei gemischter Hyperlipidämie handelt es sich um erhöhte Werte von Low-Density-Lipoprotein-Cholesterin (LDL-C) und triglyceridreichen Lipoproteinen. Triglyceridreiche Lipoproteine (einschließlich Chylomikronen, Very-Low-Density-Lipoproteine (VLDL) und Restcholesterin) spielen eine wichtige Rolle bei der Entstehung von Arteriosklerose. Es gibt keine wirksame Behandlung für gemischte Hyperlipidämie.
Bates ist dafür bekannt, den Triglyceridspiegel (TG) zu senken, allerdings ist die Senkung begrenzt. Gleichzeitig haben TG-senkende Medikamente wie Bates (wie Eicosapentaenessigsäure usw.) keinen signifikanten Einfluss auf das Risiko einer durch erhöhten Restcholesterinspiegel verursachten Arterienverkalkung. Darüber hinaus haben frühere Studien an Patienten, die bereits Statine einnehmen, gezeigt, dass kombinierte TG-senkende Medikamente das Risiko kardiovaskulärer Ereignisse nicht senken. Diese Faktoren erschweren die Behandlung einer gemischten Hyperlipidämie erheblich.
ANGPTL3 (Angiopoietin-ähnliches Protein 3) reguliert den Lipid- und Lipoproteinstoffwechsel, einschließlich TG und nicht-hochdichtem Lipoproteincholesterin (HDL-C), indem es die von Lipoproteinlipase, Endosepiase und LDL-Rezeptor (Low Density Lipoprotein) abhängige hepatische Lipoproteinaufnahme reversibel hemmt. Es wurde festgestellt, dass die inaktivierte Variante von ANGPTL3 zu einer erhöhten Aktivität der Lipoproteinlipase und Endosepiase führt, was wiederum in den meisten Fällen zu niedrigen Plasmalipoproteinspiegeln führt. Dazu gehören triglyceridreiche Lipoproteine (d. h. Chylomikronen, Restcholesterin, VLDL, Lipoprotein mittlerer Dichte [IDL]), LDL, HDL, Lipoprotein (a) und deren Cholesterinkomponenten. Heterozygote Menschen mit dieser Variante haben ein um etwa 40 % reduziertes Risiko für Arterienverkalkung, und es wurden keine nachteiligen klinischen Phänotypen festgestellt. ANGPTL3 wird in der Leber exprimiert und auf seine mRNA abzielende Gen-Silencing-Therapien, sogenannte Small Interfering RNA (siRNA)-Medikamente, sind eine vielversprechende Hybridbehandlung für Hyperlipidämie.
Am 12. September 2024 veröffentlichte das New England Journal of Medicine (NEJM) eine ARCHES-2-Studie, die bestätigte, dass das siRNA-Medikament Zodasiran die TG-Werte bei Patienten mit gemischter Hyperlipidämie signifikant senkte [1]. ARCHES-2 ist eine doppelblinde, placebokontrollierte Dosisbereichsexperimentierstudie der Phase 2b. Insgesamt wurden 204 Patienten mit gemischter Hyperlipidämie (Nüchtern-TG-Werte 150–499 mg/dl, LDL-C-Werte ³70 mg/dl oder Nicht-HDL-C-Werte ³100 mg/dl) in die Studie aufgenommen. Sie wurden in die Zodasiran-Gruppen 50 mg, 100 mg, 200 mg und Placebo-Kontrollgruppen aufgeteilt. Die Patienten erhielten in Woche 1 und 12 subkutane Injektionen und wurden bis Woche 36 nachbehandelt.
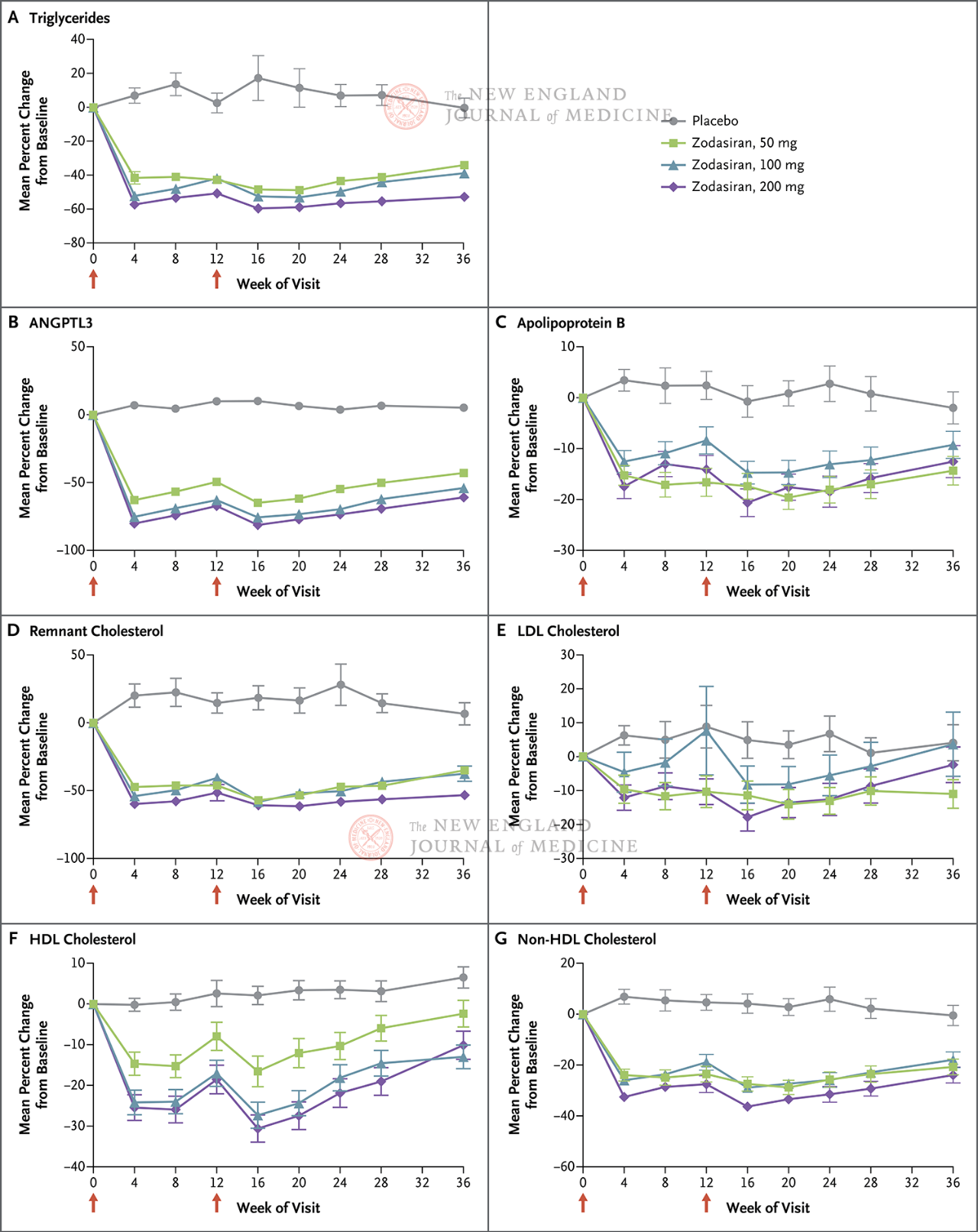
Der primäre Endpunkt war die prozentuale Veränderung der TG-Werte vom Ausgangswert bis Woche 24. Die Studie ergab, dass die TG-Werte in der Zodasiran-Gruppe bis Woche 24 dosisabhängig signifikant reduziert waren (die TG-Werte in jeder Dosisgruppe sanken im Vergleich zur Placebogruppe um 51, 57 bzw. 63 Prozentpunkte) (P<0,001 für alle Vergleiche). ANGPTL3 sank ebenfalls um 54, 70 bzw. 74 Prozentpunkte. Die Nicht-HDL-C-Werte sanken um 29, 29 bzw. 36 Prozentpunkte, die Apolipoprotein-B-Werte um 19, 15 bzw. 22 Prozentpunkte und die LDL-C-Werte um 16, 14 bzw. 20 Prozentpunkte. Diese Ergebnisse hielten bis zur 36. Woche an. In Woche 24 wurde Zodasiran
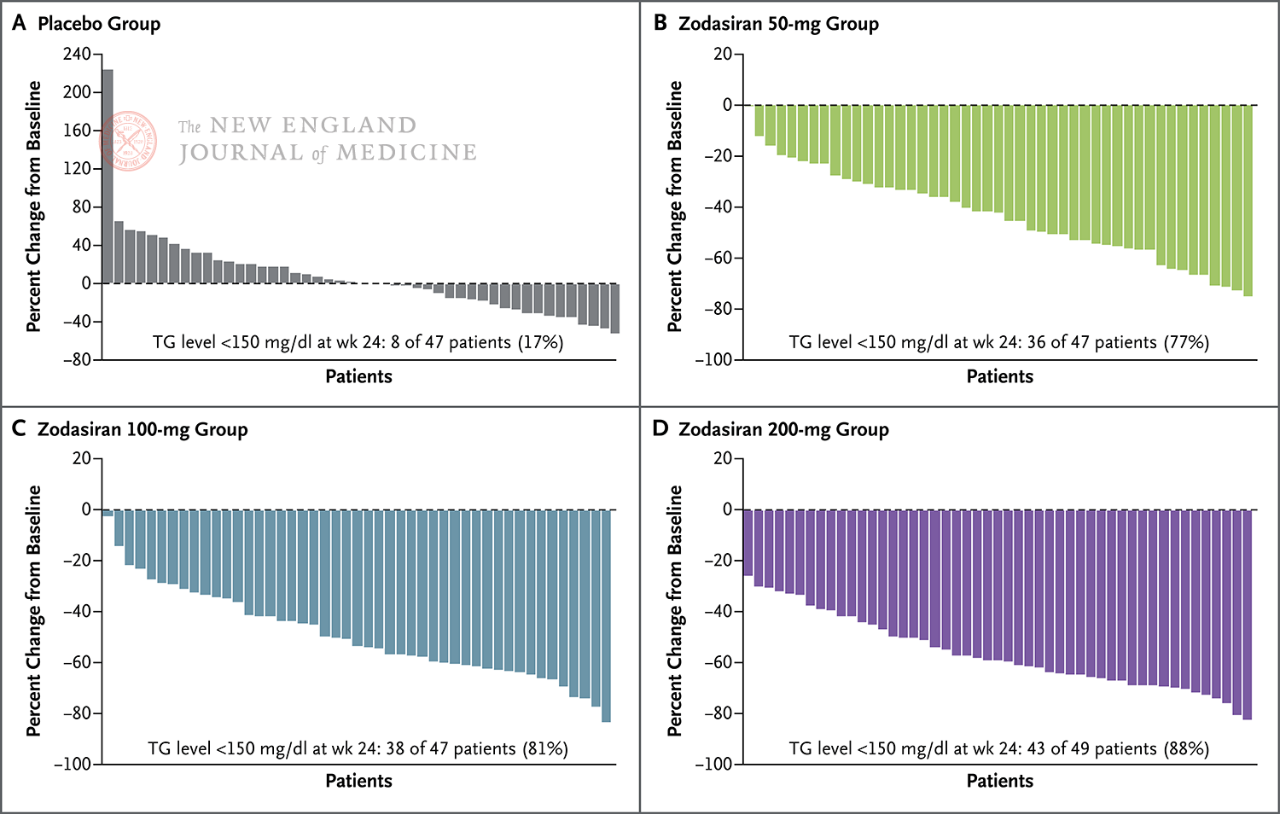
Bei 88 % der Patienten in der 200-mg-Gruppe war der Nüchtern-TG-Spiegel in den Normalbereich gefallen.
Rote Pfeile an den Tagen 1 und 12 zeigen die Verabreichung von Zodasiran oder Placebo an.
Die Nüchtern-TG-Werte sanken in Woche 24 auf den Normalwert (150
mg/dl oder weniger)
Jede Säule repräsentiert einen Patienten.
Die Studie zeigte außerdem, dass Zotasiran in allen Dosierungsgruppen sicher war. Nur zwei Patienten brachen die Studie aufgrund von Nebenwirkungen ab (einer in der Placebogruppe und einer in der 100-mg-Zotasiran-Gruppe). Alle schwerwiegenden Nebenwirkungen in der Zotasiran-Gruppe verschwanden bis zum Ende der Studie, und in der Placebogruppe gab es einen Todesfall. Die einzige besorgniserregende Nebenwirkung war ein Anstieg des HBA1c-Spiegels in der 200-mg-Zotasiran-Gruppe im Vergleich zur Placebogruppe (mittlere Veränderung vom Ausgangswert bis Woche 24 [±SD]: 0,38±0,66 % vs. -0,03±0,88 % bei Patienten mit vorbestehendem Diabetes). Bei Patienten ohne Diabetes lag der Anstieg bei 0,12±0,19 % vs. -0,03±0,19 %).
Insbesondere wurden fast alle Patienten in der Studie (96 %) mit Statinen (davon 37 % Hochdosisstatine) behandelt, 1 % mit einem Inhibitor des Proprotein-konvertierenden Enzyms Subtilysin 9 (PCSK9i) und 21 % mit Fibraten. Daher wurden durch die zusätzliche Gabe von Zodasiran zum aktuellen konventionellen Behandlungsschema immer noch erhebliche lipidsenkende Effekte erzielt, was ein neues Schema für die zukünftige Behandlung der gemischten Hyperlipidämie darstellt.
In der Studie senkte die Maximaldosis von 200 mg Zotasiran in Woche 24 den Restcholesterinspiegel im Vergleich zu Placebo um 34,4 mg/dl. Basierend auf aktuellen Modellen wird erwartet, dass diese Senkung schwere kardiale Nebenwirkungen um 20 Prozent reduziert. Zotasiran hat das Potenzial, als Monotherapie für alle Lipoproteinkomponenten eingesetzt zu werden, um das Risiko kardiovaskulärer Ereignisse bei Patienten zu senken. Weitere Forschung ist daher notwendig, um das Potenzial dieses Medikaments zur Senkung des Risikos atherosklerotischer Erkrankungen zu ermitteln.
In der doppelblinden, randomisierten, placebokontrollierten MUIR-Studie der Phase 2b, die gleichzeitig im NEJM veröffentlicht wurde, wurde ein weiteres siRNA-Medikament, Plozasiran, zur Behandlung von gemischter Hyperlipidämie eingesetzt [2]. Plozasiran soll die Expression von APOC3, dem Gen, das für Apolipoprotein C3 (APOC3), einen Regulator des TG-Stoffwechsels, kodiert, in der Leber reduzieren und dadurch den TG- und Restcholesterinspiegel senken. Die in der Studie beobachteten Senkungen der TG- und Restcholesterinspiegel ähnelten denen der ARCHES-2-Studie. Daher wird spekuliert, dass die beiden Medikamente bei Patienten mit gemischter Hyperlipidämie eine ähnliche Wirkung hinsichtlich der Senkung des Triglycerid-reichen Lipoproteins und des Restcholesterins haben.
Die Ergebnisse der beiden siRNA-Studien zeigen, dass es sich hierbei um eine sehr vielversprechende Medikamentenklasse handelt, die neue Optionen für die Behandlung gemischter Hyperlipidämie eröffnen und die kardiovaskulären Ergebnisse bei Patienten verbessern wird.
Veröffentlichungszeit: 15. September 2024